在接受治疗的8例患者中,研究人员观察到PD1-19bbz具有出色的临床安全性和有效性。有87.5%(7/8)的患者获得疾病完全缓解的效果,其中5例无癌生存已超过1年。“我们治疗的都是传统放化疗无效或治疗后反复复发的病人,这个临床结果证明这五年半的付出都是值得的。”
8月31日,国际著名科研期刊《自然》(Nature)在线刊登华东师范大学生命科学学院科研团队题为“Non-viral, specifically targeted CAR-T cells achieve high safety and efficacy in B-NHL”的最新成果。该研究首次报道了全新一代非病毒定点整合CAR-T技术的开发及其治疗复发难治性非霍奇金淋巴瘤的临床试验成效。
这一原创性研究由华东师范大学生命科学学院张楫钦、刘明耀、杜冰、李大力团队,浙江大学医学院附属第一医院黄河团队和上海邦耀生物科技有限公司合作完成。

《自然》在线刊登华东师大生命科学学院科研团队成果
《自然》资深编辑Victoria Aranda评论说,这项研究工作开展了全面系统的临床前研究,成功开发了非病毒定点整合CAR-T疗法,并取得了令人鼓舞的早期临床试验结果。
审稿人之一、美国加利福尼亚大学 Justin Eyquem 教授评论称,这项研究报道了首个PD1下调定点整合型CAR-T细胞的临床试验。研究人员在临床治疗中观察到了高比例的肿瘤完全缓解率,且未发现严重的毒副作用,这一令人惊喜的结果显示出该CAR-T疗法具有出色的临床安全性和有效性。研究人员同时也证明了非病毒定点整合T细胞治疗在临床应用的可行性。这一技术创新为未来更多基因靶向修饰CAR-T疗法的发展奠定了坚实的基础,对领域发展具有重要的推动作用。
5年半 实现CAR-T技术的创新升级

该研究第一作者、共同通讯作者张楫钦副研究员
“以往肿瘤治疗的思路都是通过药物直接去杀伤肿瘤细胞,而近些年越来越多的研究发现可以通过提高免疫细胞的功能去杀伤肿瘤,而且这种治疗方式可能带来颠覆性的疗效。在我看来,这是一个振奋人心的研究方向。”该研究第一作者、共同通讯作者张楫钦副研究员介绍说。
近年来,在全球流行的CAR-T(Chimeric antigen receptors modified T cells,CAR-T )治疗就是这样一种免疫细胞疗法。与传统抗癌药物不同,它是将患者体内的T淋巴细胞分离出来,经过体外“人工改造”后回输至患者体内,用以杀伤癌细胞。
但放眼全球,CAR-T治疗在技术层面仍存在较大的提升空间,尤其目前主要通过病毒感染方式进行CAR-T细胞制备,存在生产成本高、制备时间长、工艺复杂、有潜在致瘤风险等问题。
“针对这些痛点,我们开发了全新的技术方法,并且通过临床试验证明了我们研发的新一代CAR-T技术是安全有效的。”张楫钦说。
通过大量的条件摸索和方法优化,研究团队利用CRISPR/Cas9基因编辑技术成功实现了CAR序列在基因组特定位点的高效整合。在经过体内外肿瘤杀伤等检测证明该技术的可行性后,团队进一步制备了靶向CD19非病毒PD1定点整合CAR-T细胞(PD1-19bbz),并最终应用于复发难治性非霍奇金淋巴瘤的临床治疗。
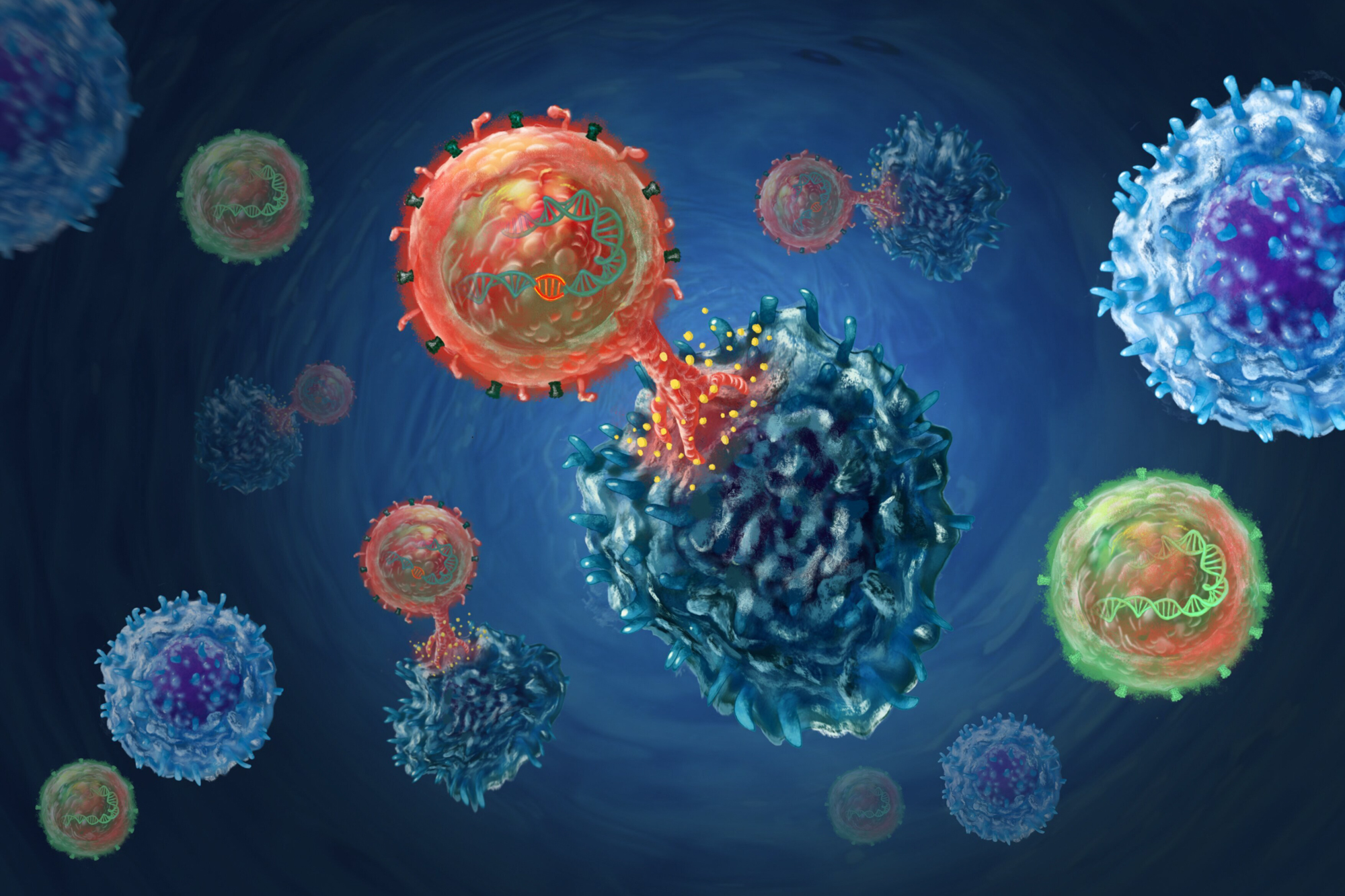
图:PD1定点整合CAR-T细胞(红色)正杀灭癌细胞(深蓝色);蓝色为活着的癌细胞,绿色为未编辑的T淋巴细胞(无法有效清除肿瘤细胞)
在接受治疗的8例患者中,研究人员观察到PD1-19bbz具有出色的临床安全性和有效性。有87.5%(7/8)的患者获得疾病完全缓解的效果,其中5例无癌生存已超过1年。
“我们治疗的都是传统放化疗无效或治疗后反复复发的病人,这个临床结果证明这五年半的付出都是值得的。”张楫钦说。
15年 从师生到联手攻关的合作者
共同参与这项创新性研究的其他几位共同通讯作者可谓阵容“豪华”,除了浙江大学医学院附属第一医院黄河教授,还包括华东师范大学生命科学学院刘明耀教授、杜冰教授和李大力研究员。
“攻读博士期间,我在生命医学研究所翁杰敏教授课题组受到了良好的科研训练,也培养了我对科学研究的浓厚兴趣,这与今天取得的成绩密不可分,我受益于学校15多年前的前瞻性布局。”张楫钦感慨道。

左起:杜冰 张楫钦 刘明耀 李大力
2007年开始,华东师大进一步深化学科布局,加强生物医学领域发展,明确主攻方向,邀请刘明耀教授回国创建全新的生命医学研究平台。
而当时,张楫钦正从同济大学本科毕业,考入了华东师大,成为生命医学研究所的首届研究生。

博士毕业后,前往上海市肿瘤研究所工作的张楫钦第一次接触了CAR-T细胞治疗这个新兴技术,他意识到利用基因编辑工具来开发新一代CAR-T技术具有巨大的潜力,因此,他想到了母校的老师们。
此时的华东师大生命医学研究所依托上海市调控生物学重点实验室这一平台,抢抓机遇,从无到有,获得迅猛发展,成为人才聚集、成果频出的调控生物学研究高地。其中,刘明耀、李大力团队在CRISPR/Cas9基因编辑方面已取得突破性成果。

华东师大团队合作报告世界首例CRISPR基因编辑治疗β0/β0型重度地贫患儿临床结果
2016年,华东师大为加强科研团队建设,新设专职科研系列岗位,也让他回归母校成为可能。张楫钦毅然决定回到华东师大刘明耀、李大力团队,作为一名专任副研究员,立志将基因编辑技术应用到CAR-T等免疫细胞治疗上,突破技术瓶颈。
“课题的定位一定要高,要做有突破性、对领域发展有重要意义的工作。”张楫钦谨记导师们的话。
“刚开始做这个课题的时候非常艰难,因为当时在T细胞中做基因编辑的人还比较少,存在许多未知和困难。”了解到杜冰教授团队在异体通用型CAR-T以及肿瘤免疫治疗的研究中取得了突破性进展后,张楫钦与杜冰教授团队开展了深入合作,充分整合各种资源,不断摸索和优化细胞的制备工艺,最终克服各种困难,实现了非病毒定点整合CAR-T的技术突破和临床转化。这项研究成果的取得也离不开上海市教委前沿科学基地和上海市调控生物学重点实验室平台的大力支持。
有组织的科研 推动重大原始创新
张楫钦还有一个身份是上海邦耀生物科技有限公司的合伙人、研发副总裁。这项研究中,作为共同通讯作者的华东师大科学家们都作为邦耀生物高级研发专家进入公司核心管理层,刘明耀教授是邦耀生物创始人,任董事长和首席科学家。
“在学校把前期的基础研究做扎实后,我们意识到这个技术真正的试金石还是临床试验,因此我们尽快跟浙江大学医学院附属第一医院、邦耀生物合作开展了研究者发起的临床试验。”张楫钦说。

近年来,华东师大通过加快变革科研范式和组织模式,实施“有组织的科研”,不断强化这种深度合作的部署和衔接。以政策引导和组织创新,鼓励科研团队与企业建立非实体研究机构,面向市场,选择与科研方向相关的领域开展紧密合作,促进原创科技成果转移转化和人才培养,同时,鼓励科研人员在不影响本职工作的前提下到企业在岗兼职,充分发挥学校基础研究的优势,将研究成果带到企业开展中试和产业化。
仅在生物制药领域,华东师大通过和上海邦耀生物科技有限公司共建上海基因编辑与疾病治疗研究中心,已产生100多项专利成果,有5个项目在8所知名医院开展研究者发起的临床试验,多个项目进入临床研究阶段。
其中,基因编辑治疗β-地中海贫血症、非病毒PD1定点整合CAR-T以及通用型CAR-T等项目已经取得优异临床效果,全球领先。
“鼓励科研人员将基础研究与应用研究深度融合,努力促进科技成果转化,”华东师范大学校长钱旭红院士说,“一方面,瞄准科技前沿,打造国家战略科技力量服务重大战略需求;另一方面,用这样的方式将优秀科研人才留在高校研究团队开展科技攻关,通过长期积累更好地推动重大原始创新。”
论文链接:https://www.nature.com/articles/s41586-022-05140-y
附科研素材:
Nature|黄河/张楫钦/刘明耀等报道全新一代非病毒定点整合CAR-T技术的突破和临床研究结果
嵌合抗原受体T细胞(CAR-T)疗法是近年来兴起的一种新型过继免疫疗法。它将患者T细胞在体外进行基因改造,使T细胞表达识别肿瘤特定抗原的单链抗体和T细胞活化的信号结构域,经过体外扩增后回输至患者体内,从而实现肿瘤的靶向杀伤。近些年,CAR-T疗法得到了迅猛的发展,目前已有六款CAR-T产品被美国食品药品监督管理局(FDA)批准用于血液肿瘤的临床治疗,标志着CAR-T技术的巨大成功1。但是,现有CAR-T技术依然存在一些尚未解决的问题,包括生产成本高、制备时间长、工艺复杂、存在潜在的安全隐患、临床安全性和有效性有待提高等。当前,CAR-T细胞的制备主要是通过慢病毒感染的方式实现的,一方面病毒通过随机整合的方式将CAR序列插入到T细胞基因组中,增加了潜在的致瘤风险2。另一方面,T细胞可能会对病毒来源的DNA产生更多的免疫反应从而阻碍CAR的持续表达3,而且病毒的工业化制备需要高昂的成本。有研究报道可以利用转座子系统来制备CAR-T细胞,以解决使用病毒载体带来的弊端4。最近,有多项研究表明结合CRISPR/Cas9基因编辑技术和使用腺相关病毒(AAV)进行模板递送,可以成功制备定点整合型CAR-T细胞5。但是,这些方法仍然无法同时解决使用病毒和随机插入这两大问题。因此,亟需开发新一代的CAR-T技术来更好地解决这些问题。
2022年8月31日,来自华东师范大学生命科学学院张楫钦、刘明耀、杜冰、李大力团队、浙江大学医学院附属第一医院黄河团队和上海邦耀生物科技有限公司合作在Nature上在线发表了题为“Non-viral, specifically targeted CAR-T cells achieve high safety and efficacy in B-NHL”的研究论文,首次报道了一种创新性非病毒定点整合CAR-T技术的开发及其治疗复发难治性非霍奇金淋巴瘤的临床试验结果。该技术可以在不使用病毒载体的情况下,利用CRISPR/Cas9基因编辑技术将CAR序列定点插入到T细胞基因组的特定位点,一步实现CAR稳定整合和内源基因调控,有效解决了目前CAR-T技术存在的使用病毒和随机插入这两大问题。
为了在T细胞中提高大片段CAR序列在基因组特定位点的整合效率,研究人员首先对制备方法进行了摸索和优化。经过比较,发现当使用同源臂长度为800bp的线性双链DNA作为模板时,可以通过同源介导修复(HDR)机制获得数量最多的CAR整合细胞。在此基础上,研究人员选择在安全位点AAVS1制备靶向CD19的定点整合型CAR-T细胞(AAVS1-19bbz),并与传统慢病毒感染的CAR-T细胞(LV-19bbz)进行比较,对该技术的可行性进行概念验证。检测结果显示CAR序列在AAVS1位点的平均整合效率为10%左右,最高可达19.8%。体外增殖、表面标志物表达、细胞因子分泌、体外肿瘤杀伤、小鼠体内肿瘤杀伤等检测表明AAVS1-19bbz与LV-19bbz具有相似的生物学特性,可以有效地杀伤肿瘤靶细胞,初步证明了非病毒定点整合CAR-T技术的可行性。
PD-L1/PD1信号通路是抑制T细胞功能的重要免疫检查点,目前针对PD-L1/PD1的抑制剂已经在多种类型的恶性肿瘤中取得了良好的疗效,也有不少研究报道了PD1敲除可以有效增强CAR-T细胞的功能6。因此,研究人员进一步地制备了靶向CD19非病毒PD1定点整合CAR-T细胞(PD1-19bbz),并开展了系统的研究。在PD1位点,CAR序列的平均整合效率可达20%左右,最高为30.3%。与之前报道相一致,PD1下调并不会影响CAR-T细胞响应肿瘤靶细胞后表面标志物表达和细胞因子分泌。为了更好地研究PD1-19bbz的功能,研究人员采用慢病毒感染结合基因编辑的方法制备了PD1敲除的CAR-T细胞(LV-19bbz_PD1-KO),并与LV-19bbz、AAVS1-19bbz和PD1-19bbz进行了平行比较。在小鼠体内肿瘤杀伤实验中,相比于其他组别,PD1-19bbz无论在PD-L1高表达还是低表达的肿瘤细胞中,都体现出更强大、更持久的杀伤效果,小鼠生存率得到显著提高。这提示PD1下调与非病毒定点整合CAR-T细胞制备方法可以联合提高CAR-T细胞的抗肿瘤功能。单细胞测序结果显示非病毒定点整合CAR-T细胞制备工艺本身能显著提高记忆性T细胞的比例,而PD1表达下调可以有效增强T细胞的抗肿瘤免疫功能,为这一现象提供了合理的机制解释。
在这些临床前研究的基础上,研究人员进一步开展了PD1-19bbz治疗复发难治性非霍奇金淋巴瘤的临床试验,对非病毒定点整合CAR-T细胞的临床安全性和有效性进行评估。在接受治疗的8例患者中,未观察到CAR-T治疗相关的神经毒性和2级以上的细胞因子风暴,证明了PD1-19bbz具有出色的临床安全性。检测结果显示PD1-19bbz回输后能在体内快速扩增并维持较长时间。接受治疗后,有87.5%(7/8)的患者获得了疾病完全缓解(CR)的效果,所有患者均对治疗响应,客观缓解率(ORR)为100%,其中有5例患者响应时间超过1年。值得一提的是,无论是针对PD-L1高表达肿瘤患者的治疗,还是在CAR-T细胞回输剂量和阳性率较低的条件下,PD1-19bbz均显示出良好的疗效,证明了其具有强大的肿瘤杀伤能力。研究人员对回输前后的CAR-T细胞进行了单细胞测序,结果显示回输前PD1-19bbz中存在较高比例的记忆性T细胞,回输后PD1低表达的CAR-T细胞具有更强的抗肿瘤功能,回输后存续的CAR-T细胞倾向于维持记忆性细胞的状态,为全面了解PD1-19bbz回输前后状态的变化并解释其临床表现提供了数据支持。
综上所述,针对CAR-T细胞治疗领域存在的痛点,本研究开发了一种全新的非病毒定点整合CAR-T技术,并通过临床试验证明了其临床治疗的安全性和有效性。利用CRISPR/Cas9基因编辑系统,该技术可以在不使用病毒载体的情况下,通过一步制备获得基因组精确整合的CAR-T细胞,同时实现CAR稳定表达和内源基因调控,有效解决了目前CAR-T技术存在的使用病毒和随机插入这两大问题。相比于其他现有CAR-T技术,该技术具有生产成本低、制备时间短、工艺简单、产品均一性高等优点,能有效增强CAR-T细胞临床治疗的安全性和有效性。本研究证明了基因编辑技术在免疫细胞治疗应用中的可行性和安全性,为解决CAR-T治疗领域现存的问题提供了新的方法和思路,对推动CAR-T技术的进一步发展有着重要意义。
华东师范大学生命科学学院张楫钦副研究员为论文第一作者、共同通讯作者,浙江大学医学院附属第一医院黄河教授为论文通讯作者,华东师范大学生命科学学院刘明耀教授、杜冰教授、李大力研究员为论文共同通讯作者。浙江大学医学院附属第一医院胡永仙教授、华东师范大学生命科学学院杨佳璇硕士为本文共同第一作者。华东师范大学为论文第一完成单位,浙江大学医学院附属第一医院为第二完成单位。本研究得到了上海邦耀生物科技有限公司、浙江大学医学院附属第一医院王东睿教授、华东师范大学吴宇轩研究员和Stefan Siwko博士的大力帮助。同时感谢参与本项临床研究的受试者及其家人的大力支持和配合。
1. Larson, R. C. & Maus, M. V. Recent advances and discoveries in the mechanisms and functions of CAR-T cells.Nat Rev Cancer21, 145-161 (2021).
2. Russo-Carbolante, E. M. D.et al.Integration pattern of HIV-1 based lentiviral vector carrying recombinant coagulation factor VIII in Sk-Hep and 293T cells.Biotechnology Letters33, 23-31 (2011).
3. Atianand, M. K. & Fitzgerald, K. A. Molecular basis of DNA recognition in the immune system.J Immunol190, 1911-1918 (2013).
4. Monjezi, R.et al.Enhanced CAR-T-cell engineering using non-viral Sleeping Beauty transposition from minicircle vectors.Leukemia31, 186-194 (2017).
5. Eyquem, J.et al.Targeting a CAR-To the TRAC locus with CRISPR/Cas9 enhances tumour rejection.Nature543, 113-+ (2017).
6. Cherkassky, L.et al.Human CAR-T cells with cell-intrinsic PD-1 checkpoint blockade resist tumor-mediated inhibition.Journal of Clinical Investigation126, 3130-3144 (2016).
来源|生命科学学院 科技处 人事处 通联|韩姬 采写|陈颖 摄影|吕安琪
编辑|张雨璐 吴潇岚 编审|郭文君
